生物人工肝的构建为疾病建模、药物开发和再生医学提供了巨大的前景。然而,现有的肝脏类器官生成方法具有局限性,包括漫长而复杂的过程(需要6-8周或更长时间),以及多能性相关的安全问题。此项研究开发了一种简单省时的方法,可在12小时内创建快速自组装微型肝脏(Rapid self-assembly mini-livers,RSALs)。RSALs表现出比之前普通肝脏类器官更大的尺寸(直径5.5 mm),具有更高的细胞活力(99%),以及增强的肝脏功能。在移植到小鼠肠系膜后,RSALs在2周内会产生功能性血管化,可有效保护90%肝脏切除术诱导的小鼠肝功能衰竭,证明了其作为生物人工肝的治疗潜力。
生物人工肝制备的一个重大挑战来自于随着类器官尺寸的增加,由于有毒代谢废物的积累和局部氧气及营养物质的供应不足,细胞坏死等问题就会出现。而肝类器官体积较大,且生长速度缓慢将进一步加剧这些问题。因此,高密度肝细胞快速组装的策略可能会解决这些问题。研究者选用纤维蛋白和琼脂糖作为载体。其中纤维蛋白是一种在凝血最后阶段发挥至关重要作用的天然聚合物。在体外模拟凝血过程,纤维蛋白基质中Arg-Gly-Asp(RGD)基序通过与细胞整合素受体的相互作用促进细胞粘附,使纤维蛋白成为增强各种细胞活性的理想支架,包括粘附、增殖和分化。由于其易于制备、可调节性、良好的生物相容性、细胞支持性和先天生物安全性,纤维蛋白在再生医学领域得到了广泛应用。此外,琼脂糖通常用于球体生成,可提供非粘附凹面,防止细胞附着在培养皿的底部。
研究者首先从C57BL/6NCrl小鼠中分离原代功能性肝细胞,并将其扩增至108个以上。即使经过15代,扩增的肝细胞仍保持其成熟的肝功能,包括糖原储存和摄取乙酰化低密度脂蛋白的能力。在琼脂糖包被的平板上,将含有肝细胞的纤维蛋白原溶液与凝血酶溶液快速混合。尽管肝细胞是在2D环境中培养的,但在添加凝血酶后仅12小时内,其就表现出了自组织成3D生物人工肝的内在能力。RSALs大小与细胞数量呈正相关,有利于RSALs标准化的建立。经体外评估,与2D环境中培养的肝细胞相比,RSALs肝功能相关基因的表达水平增加或相当,包括白蛋白(ALB)、转铁蛋白、甲状腺素运载蛋白(TTR)等(图1)。特别是Cyp3a11,其编码药物代谢酶细胞色素P450 3A11,在RSALs中的表达显著高于2D培养肝细胞。这些结果表明RSALs中的肝细胞具有增强的药物代谢能力。此外,研究者还观察到RSALs保留了摄取二酰化乙酰化低密度脂蛋白(DiI-ac-LDL) 能力。这些数据进一步支持了肝细胞可以在RSALs内维持其肝功能的观点。
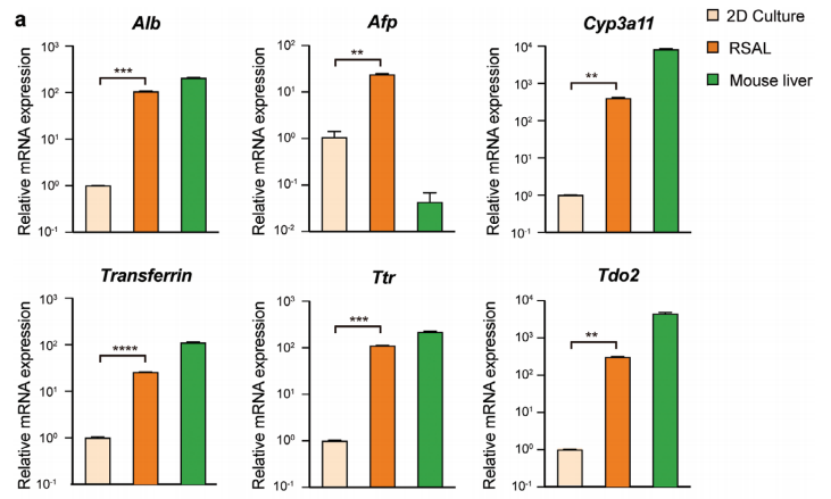
图1 RASLs与2D培养肝细胞肝功能基因表达对比
血管的生成是类器官移植到机体内能否分化与增殖的重要因素,它能够向细胞输送氧气和营养物质,并从细胞中清除代谢副产物和废物,从而维持人工肝的存活率和功能。在这项研究中,将RSALs移植到小鼠肠系膜2周后,RSALs在肠系膜内保持完整,证明了其在体内的长期生存能力。肉眼、荧光素标记、CD31免疫组化与免疫荧光染色(内皮细胞标志物)观察均显示RSALs在移植后发生了新血管的形成,并存在血流(图2),表明RSALs血管系统和宿主小鼠之间存在功能性联系,从而延长了肝细胞在RSALs内的存活时间,增强了它们的肝脏功能。
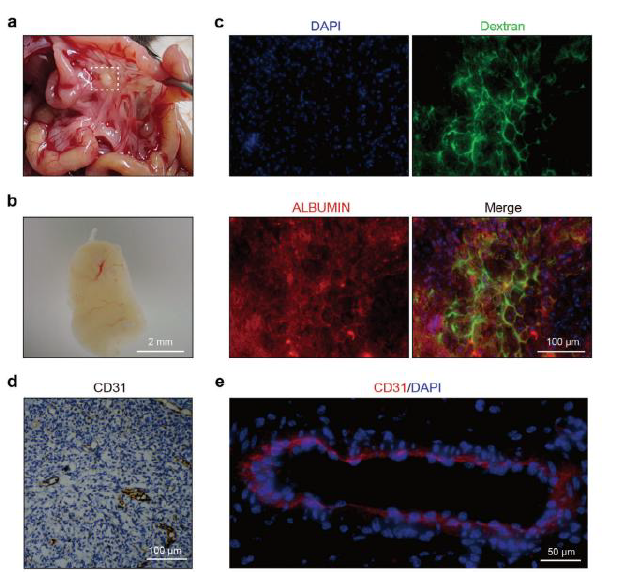
图2. 体内新生血管和长期维持的RSALs。a, b)移植后14天RSALs的肉眼观察。c)输注葡聚糖显示功能血管的形成,红色荧光显示白蛋白的表达。d)小鼠RSALs中CD31免疫组化染色。e)小鼠RSALs中CD31免疫荧光染色。
在体内研究中,移植2个月后,研究者对宿主肝脏进行了90%的肝切除,以模拟终末期肝衰竭。空白组和假手术组中,88%和100%的小鼠分别在90%肝切除后40小时内死亡,而移植RSALs的小鼠寿命显著延长(图3)。尽管RSALs在移植60天后也保持了白蛋白的表达,对RSALs切片分析显示切片中没有Ki67+细胞,表明肝细胞在移植后60天后停止了体内增殖。在肝功能生化检测方面,与假手术组相比,血清ALB浓度显著增加,球蛋白(GLB)、丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST)等血清水平降低,表明RSALs移植组的肝脏损伤显著减少,这与RSALs移植小鼠的存活率显著提高相关。研究者对小鼠的血清氨基酸浓度进行了分析,与接受假手术的小鼠相比,接受RSALs移植的小鼠的氨基酸水平显著降低,表明氨基酸代谢能力的恢复。
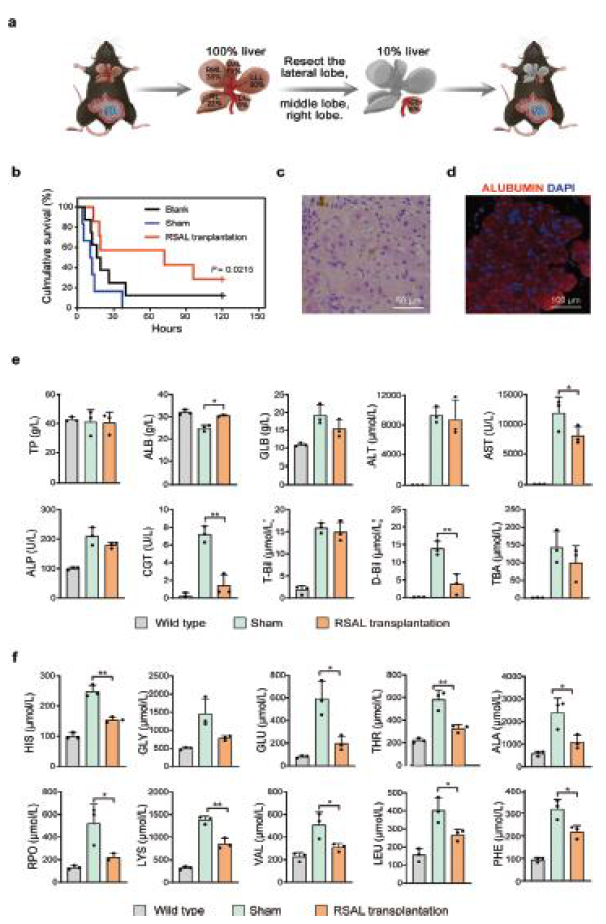
图3 RSALs移植可挽救90%的肝切除小鼠。a)90%肝切除术示意图。b) 野生型C57BL/6NCrl小鼠(n=9)、假手术C57BL/6NCrl小鼠(n=7)、RSALs移植C57BL/6NCrl小鼠(n = 7)90%肝切除后的生存曲线。c) C57BL/6NCrl小鼠肝切除90%后存活至第5天RSALs的HE染色。d) RSALs白蛋白免疫荧光染色。e) 野生型C57BL/6NCrl小鼠、假手术C57BL/6NCrl小鼠和RSALs移植C57BL/6NCrl小鼠90%肝切除术后2天血清总蛋白、白蛋白、球蛋白、丙氨酸转氨酶、天冬氨酸转氨酶、谷丙转氨酶、碱性磷酸酶、γ -谷氨酰转肽酶、总胆红素、直接胆红素、总胆红酸水平的变化。f) 野生型C57BL/6NCrl小鼠、假手术C57BL/6NCrl小鼠和RSALs移植C57BL/6NCrl小鼠在90%肝切除术后2天的血清氨基酸水平。
这项研究表明,肝细胞的快速自组装方法能够作为体内肝脏支持系统,有效地补偿肝损伤期间丧失的肝功能,从而为肝脏再生医学提供新的选择。